DNA reparation mechanisms as therapeutic target Mecanismos de reparación del ADN como diana terapéutica
Chemotherapy and radiotherapy treatments are the main procedures currently used for cancer therapeutics. They are based on the production of lethal and sublethal damage on neoplastic cell’s DNA to cause his death. The results obtained in terms of survival with these therapies are increasing every day, but its curative potential its often limited by intrinsic radio-resistance factors of the neoplastic cells.. So, since the DNA damage repair pathways have been discovered, they became potential targets to afford radio sensitization of tumor therapeutic.(1)
Repair pathways:
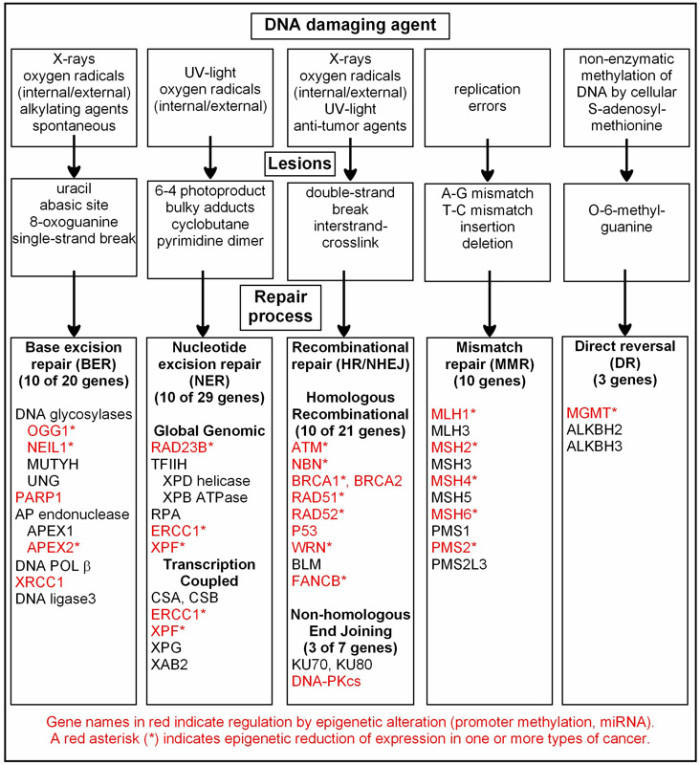
Some of those mentioned reparation mechanisms are:
Mismatch repair (MMR),
Repair and excision of bases (BER),
Nucleotide excision repair (NER),
Homologous recombination (RH),
Non-homologous end joining (NHEJ).
Among them, the three most important mechanisms are: base excision repair (BER), non homologous end joining (NHEJ) and homologous recombination (HR), which are probably responsible for most of the damage repair. The first repairs simple string breaks,
and the other two are both involved in double breaks reparation.
Both lesions are those that primarily produce the lethal radiation-induced lesions. That is why due to the importance of these three pathways, they have received more attention as potential targets of cell sensitization.
Therapeutic targets:
Repair pathways previously listed are composed of different molecules, which we will set as our therapeutic targets. Two of this targets that are being studied nowadays are the BRCA1 and the AZD7762.
BRCA1 is a gene, which encodes a protein with the same name, present in many tumors such as breast, ovarian and prostate. Reduced expression of BRCA1 in a breast cancer cell line, determine a great sensitivity to cisplatin and etiposido, which makes us think that if we inhibit this molecule in tumors with over expression of this protein, we are also increasing the treatment’s effects.(2) This is because BCRA1 is involved in NER, NHEJ and MMR pathway, so by inhibiting of BCRA1 we will be increasing the damage.
Another molecule that is currently been studied, but not as well known as the previous molecule, is the AZD7762, an inhibitor of CHK1 and CHk2, which are in charge of controlling the genetic damage, in check points at S and G2 phases of the cell cycle. The inhibition of Chk1 and Chk2 by the AZD7762, boosts the activity of Gemcitabine and Irinotecan,(3) because of these kinases are responsible for:
Phase S: repairs DNA damage
Phase G2: they hold the cell at check point, so the DNA can be repaired, or if the damage is not viable, provoke apoptosis.
Therefore, if we inhibit this kinases with AZD7762, the DNA damage caused by Gemtamicine and Irinotecan, can’t be repaired and cell dies.
Besides these examples there are other molecules that are also being investigated to be used as target for cancers treatment. Some examples are, ERCC1, RRM1 (4), and also growth factors as EGFR. These molecules open doors towards an improvement of the current chemotherapy and radiotherapy treatments, and the consequent improvement of the patient’s survival.
References:
Timothy J. Jorgensen. Enhancing radiosensitivity Targeting the DNA repair pathways. Cancer Biol Ther. 2009 Apr;8(8):665-70. Epub 2009 Apr 27.
Cobo Dols M., Gil Calle S., Villar Chamorro E., Alés Díaz I., Montesa Pino A., Alcaide García J. et al . Nuevas perspectivas en el tratamiento del cáncer de pulmón no microcítico: farmacogenómica. Oncología (Barc.) [revista en la Internet]. 2006 Feb [ci
Zabludoff SD1, Deng C, Grondine MR, Sheehy AM, Ashwell S, Caleb BL, et al. AZD7762, a novel checkpoint kinase inhibitor, drives checkpoint abrogation and potentiates DNA-targeted therapies. Mol Cancer Ther. 2008 Sep;7(9):2955-66. doi: 10.1158/1535-7163.MC
R. Rosell, M. Cobo, D. Isla, C. Camps and B. Massuti. Pharmacogenomics and gemcitabine. Ann Oncol (May 2006) 17 (suppl 5): v13-v16.
Author: Xanthe Harvey
4º Course, Medicine. Granada University
Los tratamientos con quimio y radioterapia son los principales procedimientos que se utilizan actualmente como terapéutica del cáncer. Se basan en la producción de daños letales y subletales sobre el ADN de la célula neoplásica para provocar su muerte. Los resultados obtenidos en cuanto a supervivencia con estas terapias son cada vez mejores pero su potencial curativo esta frecuentemente limitado por factores de radioresistencia intrínsecos de las células tumorales. Por eso Desde que se descubrió que los tumores presentaban vías de reparación frente al daño radioinducido del DNA estas se convirtieron en potenciales dianas terapéuticas para la radiosensibilización del tumor.(1)
Vías de reparación:
Algunos de esos mecanismos de reparación mencionados son:
Reparación missmatch (MMR),
reparación y escisión de bases BER,
reparación y escisión de nucleótidos (NER),
recombinación homologa (RH),
recombinación de bases no homólogas (NHEJ).
Entre ellos la reparación los tres más importantes son escisión de bases , recombinación no homóloga y recombinación homóloga son probablemente los responsables de la reparación de la mayoría del daño. El primero repara las roturas simples de cadena y las otras dos, están implicadas en la reparación de las roturas dobles de cadena.
Ambas lesiones son las que principalmente producen la letalidad de las lesiones radioinducidas. Por eso debido a la importancia de estas tres vías de reparación, son las que mayor atención han recibido como potenciales dianas de sensibilización celular.
Dianas terapéuticas
Las vías de reparación anteriormente enumeradas están compuestas por diferentes moléculas, las cuales vamos a tener como objetivo a tratar. Dos de las dianas implicadas en la reparación que mas se están estudiando actualmente son el BCRA1 o el AZD7762.
El BRCA1 es un gen que codifica una proteína con el mismo nombre, presente en muchos tumores tales como el de mama, ovario y próstata. La expresión reducida de BCra1 en una linea celular de cáncer de mama determino una gran sensibilidad a Cisplatino y Etoposido, lo cual nos hace pensar que si inhibimos la expresión de este gen en los tumores en los que se encuentra sobreexpresado también aumentaremos las repuesta.(2) Esto se debe a que interviene en el sistema NER, NHEJ y en la vía MMR, por lo que al inhibirla estaremos aumentando el daño.
Otra molécula en estudio actualmente, pero no tan conocida como la anterior, es el AZD7762, un inhibidor de CHK1 y CHk2 que son las encargadas de controlar el daño genético producido, en los puntos de control de las fases S y G2 del ciclo celular.(3) Esto potencia la actividad de la Gemcitabina y el Irinotecan, ya que las kinasas que inhibimos se encargarían de:
En fase S: Reparación de daños del ADN
Fase G2, mantenerla parada en el punto de control para que se puedan reparar los daños si son viables, o entrar en apoptosis si no se reparan.
Por tanto, si inhibimos estas kinasas con AZD7762, el daño celular provocado por la Gemtamicina y el Irinotecan ya no puede ser reparado y la célula entra en apoptosis.
Además de estos ejemplos existen otras moléculas que también se están investigando para ser usadas como diana terapéutica contra el cáncer como el ERCC1 o el RRM1(4), e incluso factores de crecimiento como el EGFR. Lo cual abre puertas hacia una mejora de los tratamientos actuales quimioterápicos y radioterápicos, y la consecuente mejora de la supervivencia de los pacientes.
Bibliografía:
Timothy J. Jorgensen. Enhancing radiosensitivity Targeting the DNA repair pathways. Cancer Biol Ther. 2009 Apr;8(8):665-70. Epub 2009 Apr 27.
Cobo Dols M., Gil Calle S., Villar Chamorro E., Alés Díaz I., Montesa Pino A., Alcaide García J. et al . Nuevas perspectivas en el tratamiento del cáncer de pulmón no microcítico: farmacogenómica. Oncología (Barc.) [revista en la Internet]. 2006 Feb [ci
Zabludoff SD1, Deng C, Grondine MR, Sheehy AM, Ashwell S, Caleb BL, et al. AZD7762, a novel checkpoint kinase inhibitor, drives checkpoint abrogation and potentiates DNA-targeted therapies. Mol Cancer Ther. 2008 Sep;7(9):2955-66. doi: 10.1158/1535-7163.MC
R. Rosell, M. Cobo, D. Isla, C. Camps and B. Massuti. Pharmacogenomics and gemcitabine. Ann Oncol (May 2006) 17 (suppl 5): v13-v16.
Autor: Xanthe Harvey
4º Curso, Grado de Medicina. Universidad de Granada